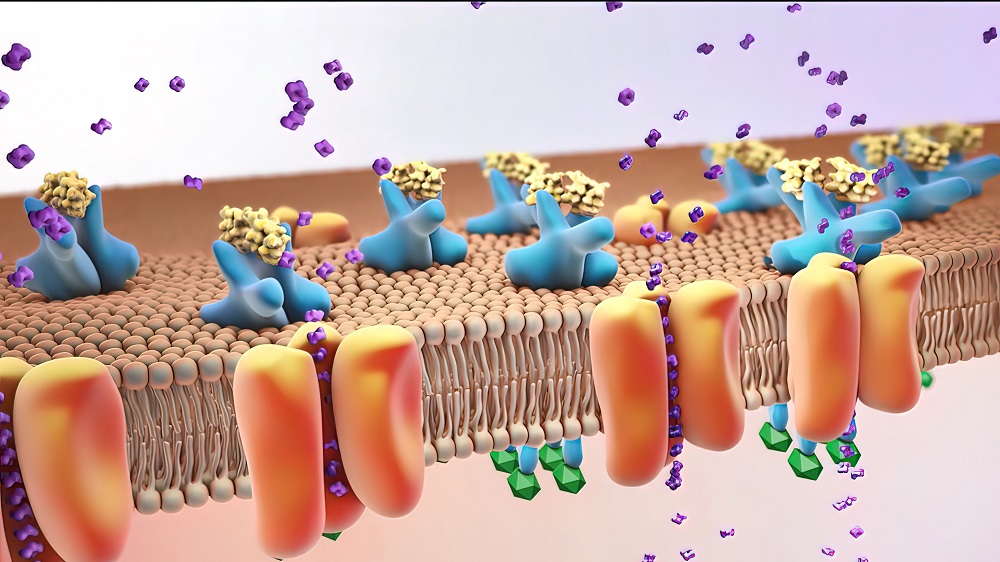
大浪淘沙,多肽正当时!
1、多肽药物发展历程
自1922年人类首次从动物胰腺中提取出胰岛素并用于治疗1型糖尿病起,全球已上市多肽药物超110种(不含仿制药),涉及罕见病、肿瘤、糖尿病、胃肠道、免疫、心血管等疾病领域。
1954年,Du Vigneaud团队首次在体外成功合成了催产素,这也是人类首个化学合成的多肽。1963年,Merrifield发明了多肽的固相合成技术,由于其合成方便、迅速,成为多肽合成的首选方法。1978年基因泰克团队宣布利用重组DNA技术生产人胰岛素,即第二代胰岛素。这三项技术为多肽合成提供了新思路从而促使各类多肽药物如雨后春笋般涌现。
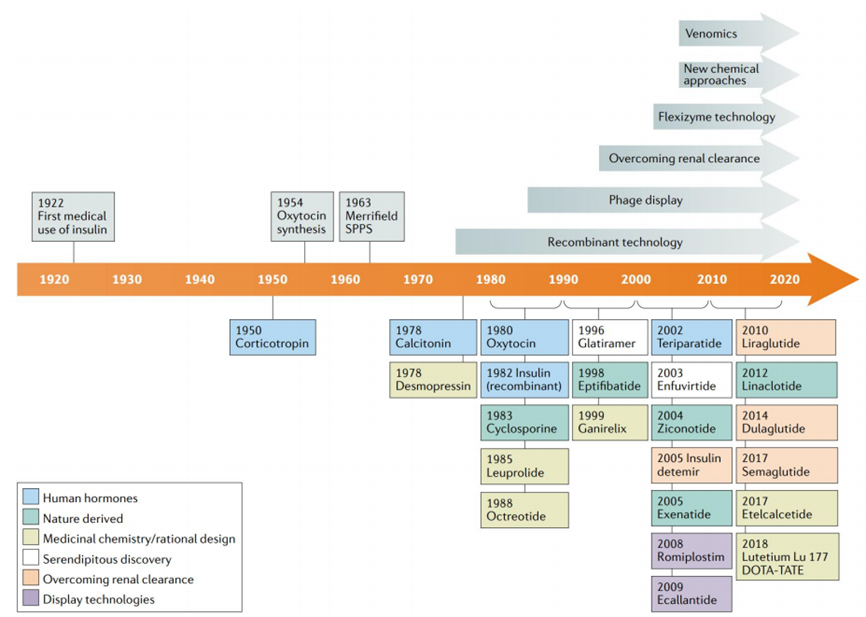
资料来源:Muttenthaler M, King GF, Adams DJ, Alewood PF.《Trends in peptide drug discovery》
据弗若斯特沙利文数据,全球多肽药物市场市场规模从2016年的568亿美元上升至2020年的628亿美元,年复合增速2.6%。预计2020年至2030年全球多肽药物市场规模的年复合增长率为8.5%,到2030年将达到1418亿美元。
2022年TOP20的多肽药物主要集中于代谢性疾病和肿瘤领域。司美格鲁肽因其长效和疗效的优势,销售额破百亿美元。根据诺和诺德2023年报,其GLP-1类药物整体销售额达1231亿丹麦克朗(约178.8亿美元),GLP-1也成为2023年全球biotech企业最关注的靶点。礼来的Zepbound在2023年11月8日获批上市,12月就迅速地出现在美国市场,两个月达1.75亿美元的销售额。全球破百亿美元的药物有多个,但GLP-1相关药物成功的链接了严肃医疗和消费医疗两类医疗市场,为聚焦慢病领域的企业提供了新的市场开拓思路。
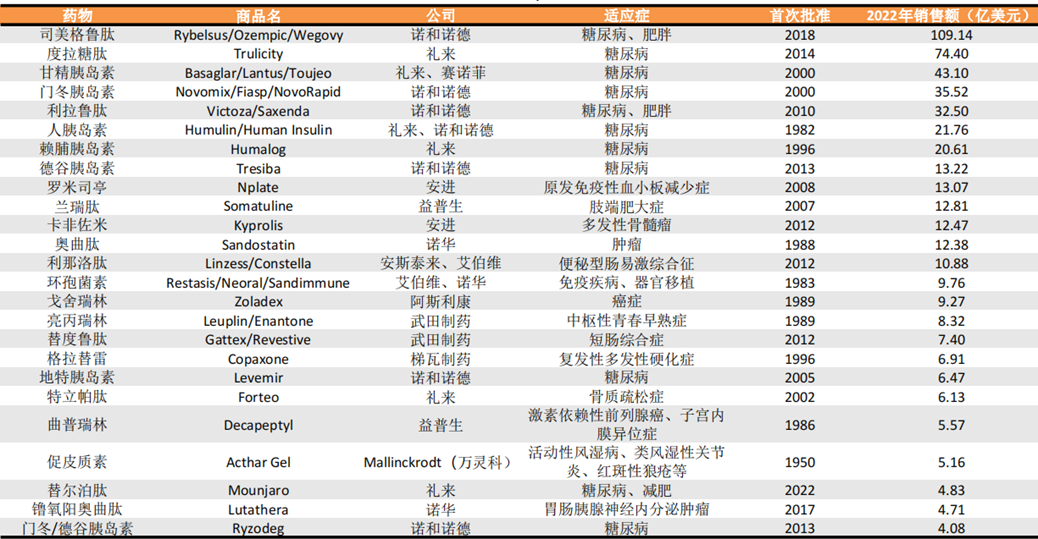
资料来源:肽研社公众号,《Trends in peptide drug discovery》Markus Muttenthaler,各公司官网
2、多肽筛选
多肽筛选是指通过不同的方法筛选出对特定靶标具有结合能力或生物活性的多肽序列。早研机构现阶段主要使用肽库筛选,通过亲和筛选、细胞筛选和固相筛选对文库中的多肽进行初筛。通过细胞表面展示进一步验证筛选,最终在模型动物进行体内验证。
筛选过程中通常使用光学检测法、代谢稳定性法和生物学检测法。光学检测法通过荧光标记或放射性同位素标记的多肽筛选技术进行。代谢稳定性法通过检测多肽对代谢的稳定程度筛选具有生物活性的多肽序列。生物学检测法通过检测多肽对生物学系统的反应来筛选具有生物活性的多肽序列。
多肽筛选方法是固定的,灵活的组合筛选可节省研发成本,但成功筛选出安全且有效的多肽药物的最终前提是原有肽库中有大量适合此类靶点的多肽序列。肽库按照多肽的组合方式可划分为重叠肽库、随机肽库、截断肽库等种类。按照肽来源可分为噬菌体展示肽库、化学组合多肽库。
噬菌体展示肽库是将人工合成编码随机多肽段的基因克隆到噬菌体载体中,通过噬菌体表位展示技术把多肽一一展示在噬菌体表面,构建一个多肽文库。依据特定的受体靶标与肽库中某些多肽的特异相互作用,从肽库中筛选出与特定靶标相结合的多肽。
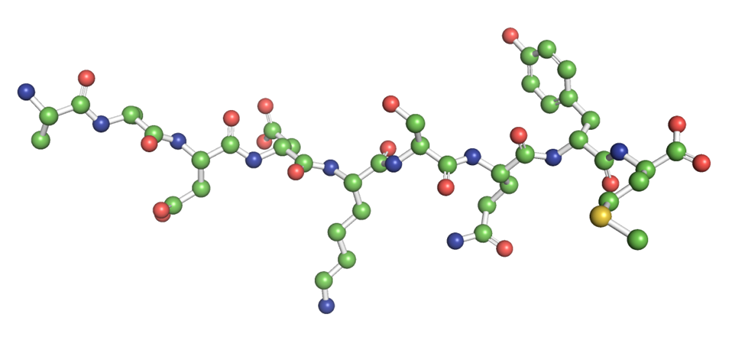
不同于噬菌体表面呈现肽库仅限于天然L型氨基酸,而化学组合肽库可包括D型氨基酸等其他异构体在内的非天然氨基酸以及额外的附加二级结构。化学组合多肽库是通过在树脂上随机排列组合形成多肽序列。例如,5肽库就会有5的5次方个五肽,9肽库就会有9的9次方个九肽。但其筛选难度极高,且建库成本极高,适用于早期AI算法筛选。
进而衍生出DNA编码的化学组合多肽库:载体树脂上随机合成多肽且同时包含DNA合成的由成千上万个多肽与DNA组合成,其中每接一个氨基酸就会对应合成几个核苷酸来编码多肽的信息。筛选时,受体靶标需要接一个荧光分子,某个多肽若与受体结合,相应的的树脂就会有荧光,以此降低化学组合多肽库筛选难度。
简单概述了多肽筛选,但实际筛选工作远远没如此简单,以上方案仅筛选出具备亲和力的多肽,而多肽是否有效还需进一步优化,涉及酰基化、酯基化、PEG化,beta-氨基酸取代、D氨基酸取代,主链氨基甲基化、二硫键替代、构象锁定(螺旋、beta-sheet)、镜像多肽、环肽(首尾环化、侧链环化)、特殊分子标记,羟基酸取代等。这些都需要科学家根据初始多肽的结构特点和期望特性进行验证修改。作为药企而非科研机构,除了考虑其成药性和药效,还必须考虑其工艺性价比,没有可接受的生产成本,化合物只能躺在早研的文件夹中。
3、多肽生产工艺
多肽合成方法可分为化学合成法和生物合成法,同时随着生物工程技术的发展,以合成生物学发展起来的新一代发酵技术和以绿色工业为代表的酶催化技术也被应用于多肽的合成。

化学合成多肽重点在于在恰当的位置和时机活化或保护氨基、羧基。化学合成法具有研发周期短、可快速生产等优点,可分为液相合成法和固相合成法,两者主要的区别源于是否使用固相载体;液相合成法发展较早,固相合成法是如今多肽合成的主流方法。液态合成多肽在均相中进行,是以 N-保护氨基酸为起始原料,逐步连接氨基酸残基的过程,可以采用分段合成的汇聚式路线。每一步反应都需要将中间体分离纯化后,再进入下一步反应,可以对中间体的结构进行跟踪和检测。但这增加生产难度,生产一个多肽分子往往需要超过百步工艺。而且分离纯化过程会产生大量的溶剂消耗,增加环境压力。
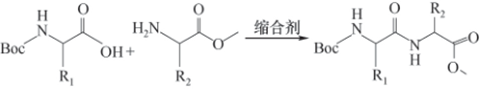
固态合成多肽是将首个保护氨基酸负载在高分子树脂(或膜材料)上,然后依次与后续的氨基酸缩合,无需进行中间体分离,通过过滤的方法即可将负载在树脂上的中间体从溶剂中分离出来,可实现自动化或半自动化生产。分离纯化过程减少,生产周期减少,溶剂消耗减少。最后,将产物从树脂上解离下来,再脱去保护基。
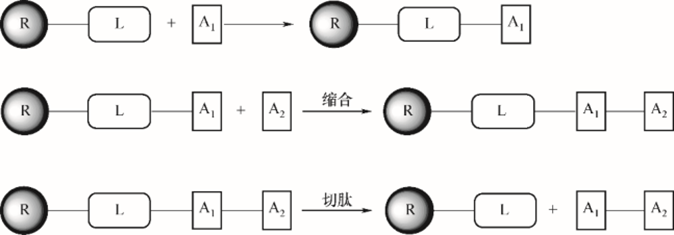
生物合成法具有定向表达强、成本低的特点,可分为天然提取法、酶解法、发酵法、基因重组法等,其中发酵法是生物合成方法的基础。
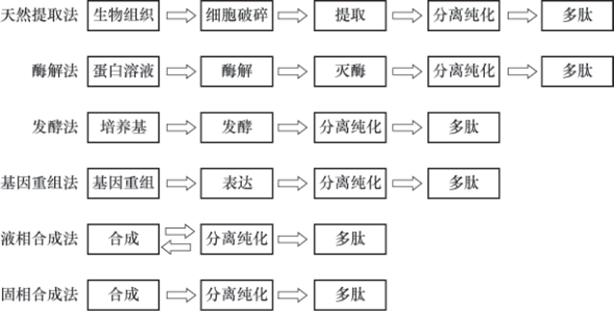
目前,多肽药物大规模生产仍存在较高壁垒:
工艺路线复杂,多肽原料药生产步骤多,使用不同的试剂、策略和方法均会导致各环节产生不同种类和量级的杂质,每个环节需要根据杂质和纯度等质量研究情况多次调整导致生产成本控制难度大。
质量控制与纯化分离难度高,合成得到的粗产品中杂质多样且复杂,在多肽药物生产中除了纯度、含量、溶剂残留等检测项目外,还需要关注与结构及合成特点相关的一些检查项目,同时需要进行生物学安全性检查。
在底层合成方法难以创新的情况下,生物和化学结合生产的工艺成为近20年的主体合成工艺,工艺创新方式具备相应的复杂性和繁琐性,哪一部分使用生物合成,哪一部分使用化学成为多肽合成工艺的拆分结合问题,需要大量研发经验加持,也成为国内多肽CDMO突破的方向。引入AI助力化学合成已在小分子早期合成领域展露头角,将AI合成引入多肽合成,具备提高工艺创新效率的可能性。
4、GLP-1
概述多肽不得不提及GLP-1相关药物,目前全球已上市多款 GLP-1 多肽类药物,包括每日注射产品(艾塞那肽、利拉鲁肽、利司那肽和贝那鲁肽等),周注射制剂(艾塞那肽微球、阿必鲁肽、度拉糖肽、司美格鲁肽、替尔泊肽和聚乙二醇洛塞那肽等),以及口服司美格鲁肽等。目前上述药物均已获批用于2型糖尿病的治疗,但其中仅有利拉鲁肽、司美格鲁肽、替尔泊肽获批肥胖减重适应症。
国内已获批减重药物主要有奥利司他和利拉鲁肽,两个产品均有各自缺点。奥利司他与其他获批减重药物相比减重效果较弱,但不良反应却更强,主要引起胃肠道不良反应。而利拉鲁肽为短效GLP-1受体激动剂,需要每天注射使用,使用较为不便,且减重效果一般。
司美格鲁肽(0.25~2.4mg,qw)可使1/3的肥胖者减轻至少20%的体重;Tirzepatide(2.5~15mg,qw)帮助超过50%的肥胖者减轻了至少20%的体重。从现有最佳减重数据来看,目前经过46周以上治疗后药物减重效果排序为礼来Retatrutide( GLP-1R/GIPR/GCGR)、礼来Tirzepatide(替尔泊肽)(GLP-1R / GIPR )、诺和诺德口服司美格鲁肽(GLP-1R)、诺和诺德司美格鲁肽(GLP-1R)、勃林格殷格翰 Survodutide( GLP-1R/GCGR )等,其相对基线时体重减轻程度可达 15%以上,目前最佳治疗数据为相对基线时体重减轻24%。
不同减重药物高剂量用药时长≥46w 的最佳减重效果对比(较基线体重下降百分比)
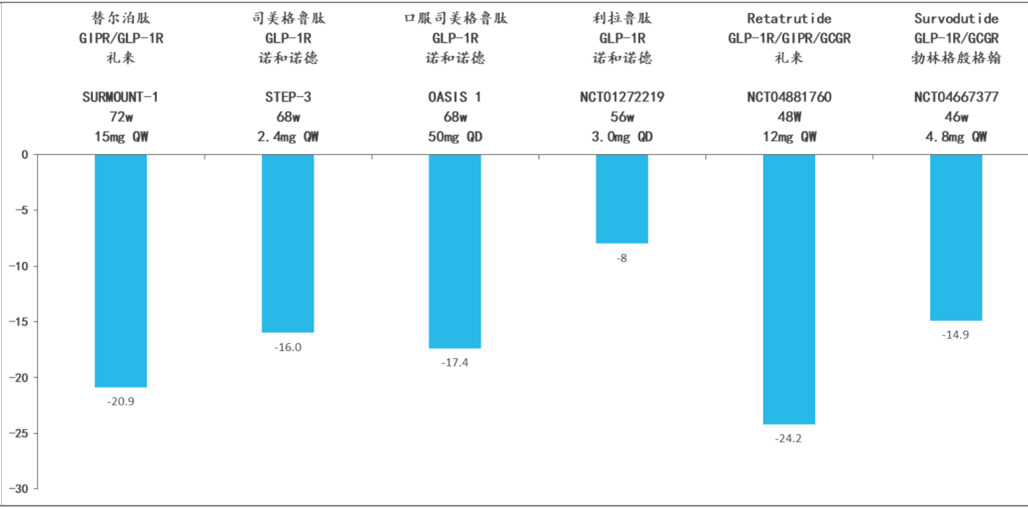
资料来源:公司官网,Pubmed,安信证券研究中心
受益于降糖与减重市场的扩展,2022年全球已获批上市 GLP-1 多肽类药物整体销售规模已达 225 亿美元规模以上,其中销售额前两位的产品 Ozempic(司美格鲁肽)、Trulicity(度拉糖肽)。Tirzepatide(替尔泊肽)作为减肥药在2023年11月上市,成为Semaglutide(司美格鲁肽)的直接竞争对手出现在减肥药市场。
全球已获批上市 GLP-1 多肽类药物销售额趋势(单位:亿美元)
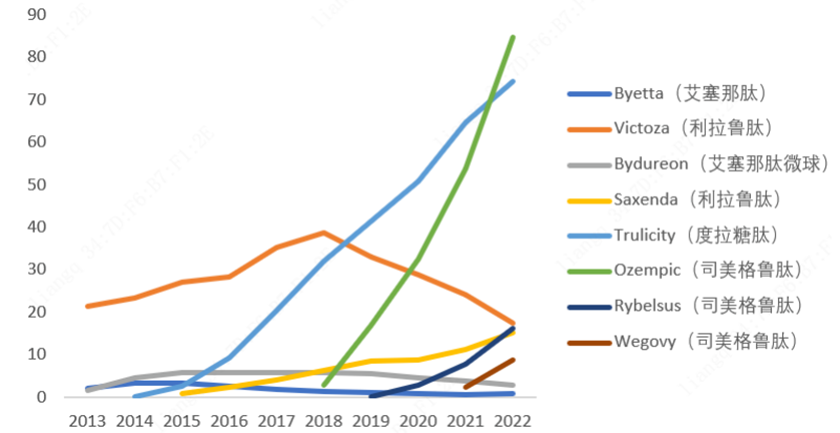
资料来源:医药魔方,公司财报,安信证券研究中心
国产 GLP-1 多肽药物研发能力稍有滞后国外,但国内多肽药物研发高潮依然持续。目前信达生物、先为达已披露数据。国产药物中信达生物IBI362 ( GLP-1R/GCGR )在第 24 周已表现出显著的减重效果(相对安慰剂组其体重减轻可达15.4%),且前期研究表明其减重效率较高;此外先为达也披露了 Ecnoglutide 的 2 期数据,第 26 周时相对基线体重减轻 14.7%,表现也相当优异。
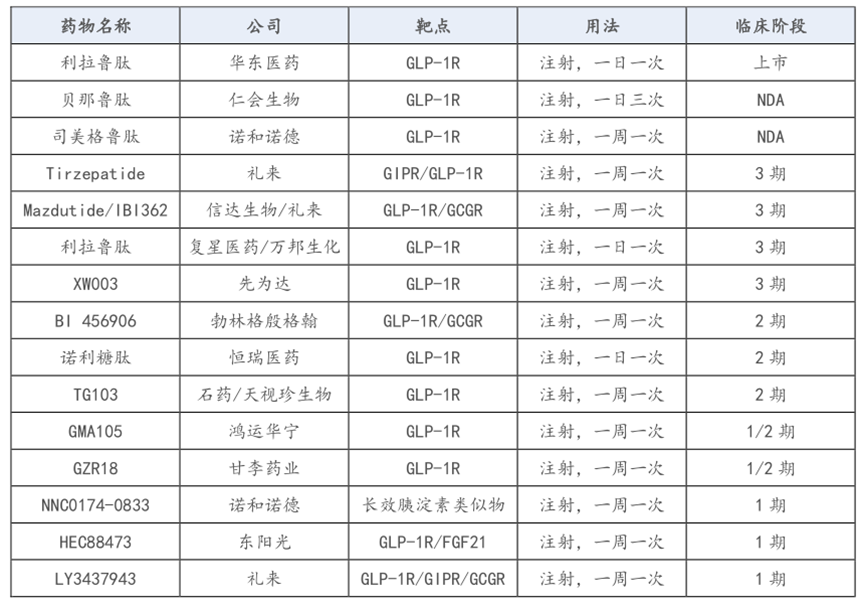
资料来源:资料来源:CDE,安信证券研究中心
GLP-1 多肽应用领域逐渐扩张,临床实验已从糖尿病、肥胖减重扩展到 NASH 等疾病。心血管疾病也将成为GLP-1药物关键的催化剂,诺和诺德的III期SELECT试验是GLP-1药物在心血管疾病领域有效的第一个关键证据。临床数据显示,与安慰剂相比,接受2.4 mg semaglutide治疗的患者的MACE (不良心血管事件,包括心血管死亡、非致命性心肌梗塞和非致命性中风)显著降低了20%,达到了其主要终点。
Tirzepatide中国布局
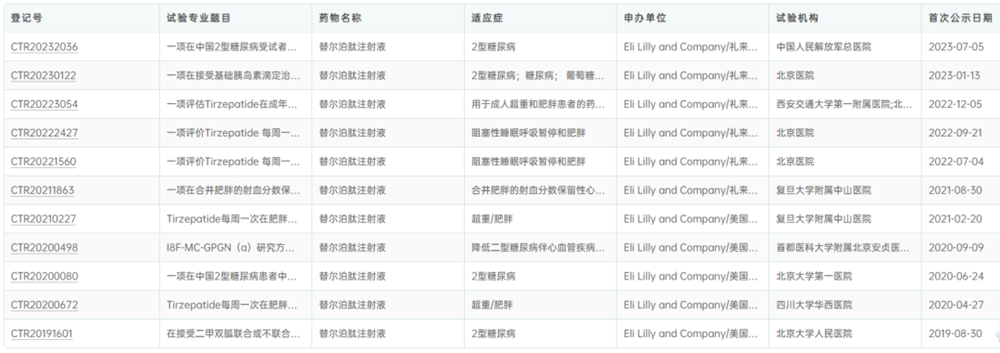
代谢类疾病和心血管疾病的有效应用,将进一步扩大GLP-1多肽药物在慢病领域的市场份额。除了心血管疾病之外,GLP-1药物也正在研究阻塞性睡眠呼吸暂停、慢性肾病、肝病、膝骨关节炎甚至阿尔茨海默病(AD)方面的潜在益处。在NASH疾病治疗领域,GLP-1 多肽类产品中诺和诺德的司美格鲁肽、阿斯利康的Cotadutide 已进入3期临床开发阶段。
目前GLP-1在阿尔兹海默症领域的临床前验证数据展示,在多类AD模型鼠上有认知改善和记忆改善。但具体作用机制依然不明确,有研究论述GLP-1 易于透过血脑屏障,通过结合并激活脑中广泛分布的 GLP-1 受体 (glucagon-like peptide 1 receptor,GLP-1R) 影响多个病理生理过程,如葡萄糖代谢、神经炎症、线粒体功能和细胞增殖等。而胰岛素抵抗和炎症是AD与Ⅱ型糖尿病的关键共同通路。GLP-1可能是通过改善线粒体功能和糖酵解、降低氧化应激水平、抗炎、抗凋亡、诱导神经发生和抑制胶质细胞增生等,发挥神经保护作用。
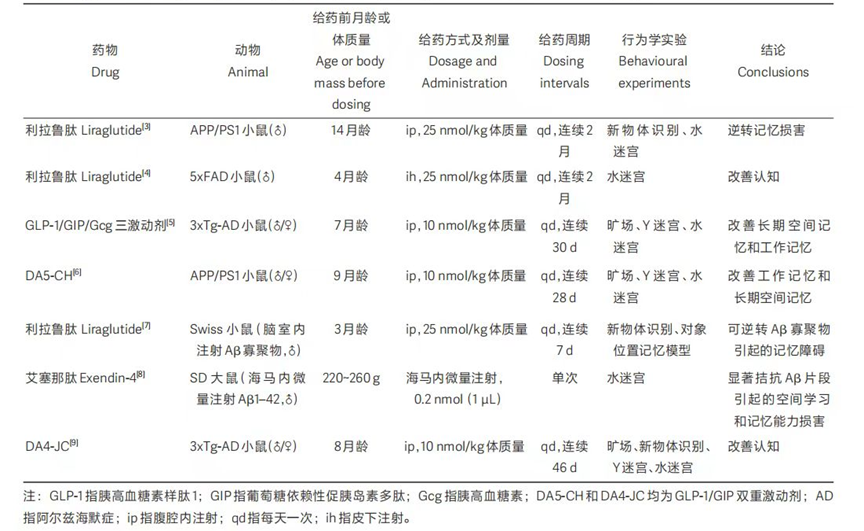
资料来源:胰高血糖素样肽 1 类似物对阿尔兹海默症的神经保护作用及机制研究进展,梅承翰, 陈蓓蓓
GLP-1 受体激动剂具有多种生物学效应,随着更多药物获批上市,GLP-1 药物市场将快速发展。适应症扩充和长效GLP-1多肽药物的普及,使得其全球销售额还会持续高水平增长。在 2016-2020 年间,GLP-1 药物在我国的销售规模从 4 亿元人民币快速增长至 16 元亿人民币。首个长效 GLP-1 药物于 2018 年在我国上市,另三种长效 GLP-1药物紧随其后上市,大幅改善的患者治疗依从性,促使我国长效 GLP-1 药物市场规模快速扩增,同时推动整体GLP-1 药物市场的发展。
根据弗若斯特沙利文数据展示,预计整体 GLP-1 药物市场将以 57.0%的复合年增长率增长,于 2025 年达到 156 亿元人民币。其中长效 GLP-1 药物细分市场在 2020-2025 年间将以 100.6%的速度增长,于 2025 年达到 107 亿元。在此之后,整体 GLP-1 药物市场将保持 26.2%的复合年增长率,并在 2030 年达到 501 亿元。
5、多肽药物前景
无论从靶点发现,多肽序列筛选还是工艺合成,多肽药物研发都有进一步发展的空间。对于国内多肽药物行业,可谓是大浪淘沙,多肽正当时。但不可否认现有多肽药物存在自身的局限性:
1. 多肽药物比小分子化药结构复杂,合成成本较高,虽然多肽固相合成技术已相对成熟,但是多肽药物合成的中试放大生产仍具有相当的难度;
2. 多肽分子易被酶降解失活,且脂溶性较差,难以透过细胞膜,所以多肽药物的半衰期较短、生物利用度较低,通常只能采用注射给药,需要频繁注射给药,患者依从性低。
GLP1药物的发现与发展具备偶然性和必然性,偶然性在于人类在希拉毒蜥的毒液中发现含有GLP-1类似物,进而有了艾塞那肽。必然性在于相关靶点和作用机制的发现在生物技术的发展下必定使得原始药物得以进一步优化成药。偶然性使得人类使用相关药物的时间提前,必然性使得从2000年FDA批准艾塞那肽上市到现状我们有大量的相关药物可以选择。靶点发现必须依靠基础研究的坚持和深入,2023年的最大话题在于GPT,它的出现将进一步改善点对点的知识交流局限性,为创新发现提供更多灵感可能性。
针对现有表征能力和计算能力,很难达到理想化化合肽库的AI筛选。但科研人员是可以通过结构功能对庞大多肽库进行分类,以此减少算力。对自然界多肽分离筛选是我国的优势方向,毕竟传统中药中有大量动物药材富含多肽成分,但现有表征主要基于蛋白组学和基因组学,并未对其功能肽成分进行识别区分。这是一个难出成果的苦力活,可基础科研本就是苦中作乐,本就是众里寻他千百度,那人却在灯火阑珊处的过程。
多肽工艺的优化离不开相关技术的提升,包括微流控技术、膜强化多肽合成技术、在线监控与自动化技术等。药物工艺开发最主要目的就是降低成本和风险,结合多肽药物疗效显著、用药剂量小、不易产生耐药性的特点,在控制风险的情况下,寻找提高产量并减少生产时间的工艺是市场需求方向。作为拥有自主定价权的创新药物,成本并非企业现在考虑的第一要素,快速的抢占现有市场是司美格鲁肽的目的,这也成为国外CDMO弯道超车的突破点,专利断崖后生产成本便是相关药企的考虑的重要因素。因而多肽工艺优化将是近10年的突破热潮和研发方向。
专利断崖是研发药企心中的一根刺。如何延长专利保护期,如何提高技术壁垒,如何扩充适应症,如何设计迭代产品,是药企考虑的重点。对于多肽药物而言,对多肽序列和类似序列专利的保护是基础,工艺和检测技术专利是延长专利和提高技术壁垒的主流途径,针对迭代设计可分为制剂优化减少给药频率,多靶点多肽,多肽偶联药物,以及药物联用。
来源于网络
近年主要通过改变多肽结构、对多肽进行修饰以及与血清蛋白融合等方法使其长效稳定。同时多肽口服制剂技术也快速发展,司美格鲁肽作的口服制剂是和SNAC一起构成的配方,在吸收的过程中,SNAC在胃部溶解局部升高胃的pH值,提高司美格鲁肽的溶解度且将胃中酸性环境改变为中性环境,使肽酶失活,避免司美格鲁肽被胃中的肽酶降解。然而,口服司美格鲁肽生物利用度依然很低,只有1-2%左右,因此口服剂量远远高于注射剂,成本增加;且口服前需空腹6小时,多种原因导致其销量不高,相较之下进一步提高注射药物的长效性和口服药物的依从性是制剂创新的重点,但总归探索出多肽口服的路径。
多靶点肽是具有靶向多个靶点、具备多种药理活性、形成不同机制间的协同增效和具备更好安全性的多肽分子。结合其渗透性优于大分子的特点,使其对一些复杂疾病如心脑血管、代谢、中枢神经系统及免疫性疾病的治疗有可能性。从风险和成本角度分析,多靶点肽与其他单一分子实体在临床开发中,原则上没有区别。
从目前角度分析,国内擅长对已知功能结构的优化和结合,多靶点肽和PDC都是随机排列组合,且不用考虑旁观者效应和偶联技术,但难点在于多结构状态的筛选。但全球进入临床阶段 (含2个上市)的多靶点肽约24个。最具代表性的多功能肽龙头企业包括Eli Lilly (礼来)、Apellis、Hammi、AstraZeneca (阿斯利康)、Amgen (安进)等,国内麦科奥特在这一领域是龙头企业。回看多特异性抗体的发展历史,多靶点肽也会出现相应的高光时期。
国内多肽企业临床管线表
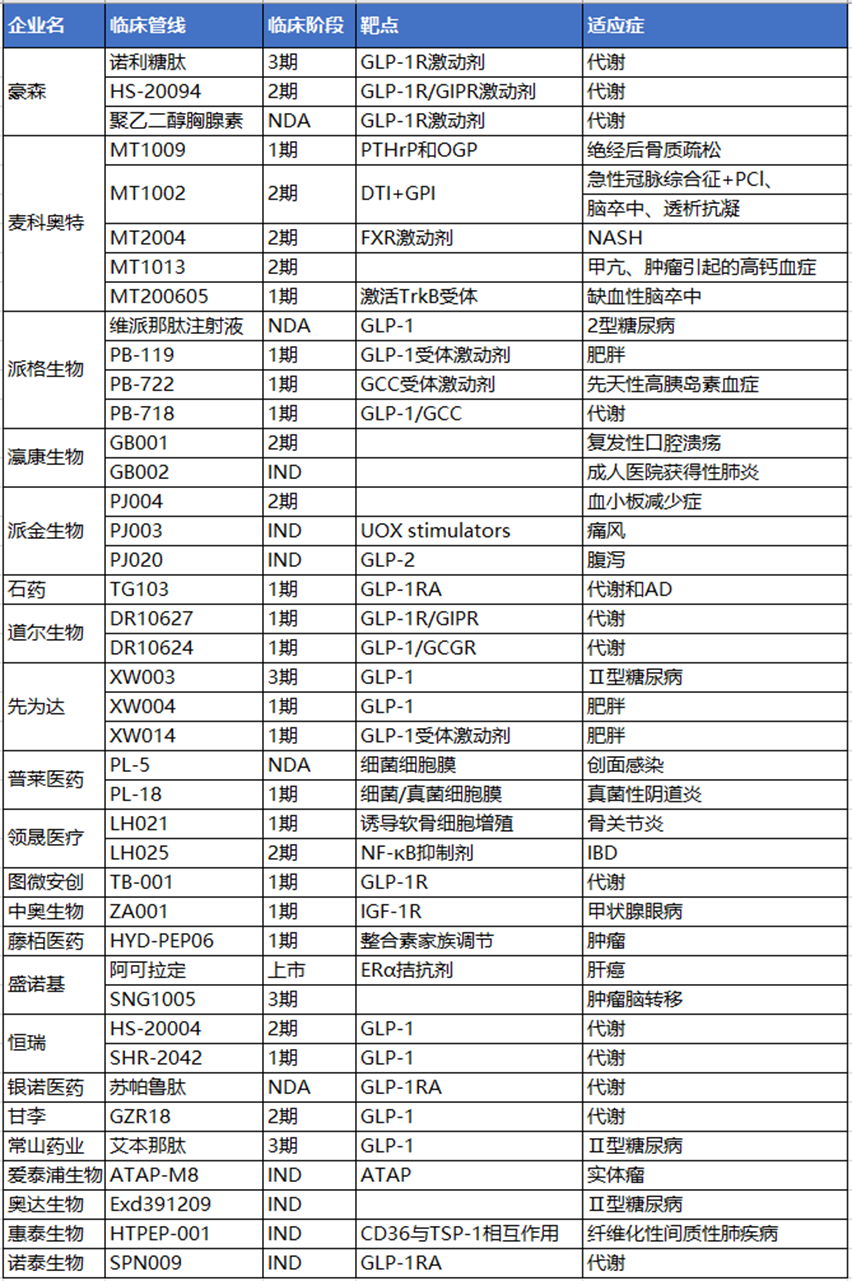
多肽偶联药物:泛指与抗体(PAC,Peptide Antibody Conjugate)、核酸 (POC,Peptide Oligonucleotide Conjugate)、多肽 (多功能肽)、核素 (RDC,Radionuclide Drug Conjugates)、小分子 (PDC,peptide drug conjugate)等偶联的多肽药物,统称为“偶联肽”。国内偶联肽是否如同ADC药物出海成功,还未可知,但不可否认的是偶联肽在神经中枢系统疾病的应用前景十分可期。
所有药物发展的趋势均是趋于复杂,因为结构简单且有效的药物已被大量开发。多肽药物分子结构也会越来越复杂,不仅仅表现在引入非天然氨基酸,或其他更多的功能基团(蛋白、小分子)等;还包括更多组合形式,环肽、双环肽,订书肽,β折叠等。近10年,当小分子在CADD和AIDD中寻找新能源,抗体在多特异性和偶联中寻找下一个神话,细胞治疗在通用性和杀伤性中寻找平衡支点,基因治疗在多基因罕见病中投石问路,虽然国内多肽研发和国外依然有不小差距,但多肽正在风口浪尖中成长为不可替代。
关于格林泰科
四川格林泰科生物科技有限公司是一家专注建设参照GLP管理标准进行新药临床前药效与药代动力学评价服务机构(CRO),在降糖减重、NASH、肝纤维化、肝硬化、PBC/PSC、糖尿病肾病、肺纤维化等代谢性疾病领域已完成多肽研究项目百余项,涉及的实验动物包括大小鼠、转基因小鼠、犬、猴等,均完成相关申报项目,积累了大量早期筛选、DMPK和正式评价研发经验和相关数据,欢迎朋友们咨询交流。